Carmen Cristina Olteanu1, Ettore Pedretti2, Giuseppa Privitera2
Articol primit la data de 11 octombrie 2011. Articol acceptat la data de 8 noiembrie 2011.
1 Spitalul clinic de urgenţă pentru copii “Grigore Alexandrescu”, Bucureşti
2 U.O. Pediatria della Val d’Arda, Piacenza (Italia)
Dr. Cristina Olteanu, Spitalul clinic de urgenţă pentru copii “Grigore Alexandrescu”, Bd. Iancu de Hunedoara Nr. 30-32, 011743 Bucureşti –Sector 1. Tel: +40-21-316.93.66 int 140.
e-mail: c_cristina_olteanu@yahoo.com
Rezumat: Este prezentat cazul unui sugar in vârstă de 5 luni cu semne de insuficienţă cardiacă şi o severă distrofie, la care ecocardiografia iniţială a depistat doar o malformaţie cardiacă simplă, respectiv defect septal interatrial larg tip ostium secundum, care a fost corectat chirurgical. La câteva zile după intervenţie au apărut semne de ischemie miocardică. S-a diagnosticat în acest context originea anormală a arterei coronare stângi din artera pulmonară, devenită manifestă urmare a scăderii presiunii pulmonare după închiderea defectului interatrial.
Cuvinte cheie: origine anormală de coronară, insuficienţă cardiacă, ischemie miocardică, defect septal interatrial
Abstract: We are presenting the case study of a 5 months old baby with heart failure and severe dystrophy, initially diagnosed with an large interatrial septal defect (ostium secundum type) only. Surgical correction was performed. After a few days, signs of myocardial ischemia became evident. Abnormal left coronary origin, from the pulmonary artery, was diagnosed, now clinically evident because of the pulmonary pressure drop after the interatrial defect closure.
Keywords: abnormal coronary origin, heart failure, myocardial ischemia, interatrial septal defect
Introducere
Originea anormală a arterei coronare stângi din artera pulmonară este malformaţia coronariană cea mai comună. Incidenţa este de 1: 300.000 de născuţi vii1. În 90% din cazuri se manifestă în prima copilarie, cu o mortalitate, în cazul când nu este recunoscută şi corectată, de aproximativ 80% în primul an de viaţă. Unele cazuri pot ajunge la vârsta adultă fără simptome, cu posibilitatea apariţiei ulterioare a dispneei, anginei, sincopei sau a morţii subite. Anomalia este descrisă in tratate ca fiind izolată, dar şi asociată cu persistenţa de canal arterial, defectul septal interventricular, tetralogia Fallot sau coarctaţia de aortă. Nu este menţionată posibilitatea asocierii cu un defect septal interatrial2,3. În prezenţa hipertensiunii pulmonare, perfuzia ventriculară poate fi adecvată in ciuda malformaţiei coronariene şi astfel să fie prevenită ischemia miocardică. În aceste condiţii, corectarea anomaliilor asociate cu scăderea ulterioară a presiunii arteriale pulmonare către normal, poate avea consecinţe catastrofale pentru irigaţia miocardică şi funcţia ventriculară stângă1. Reimplantarea directă a originii arterei coronare stângi în aortă (cu un buton de arteră pulmonară în jurul originii) este abordarea terapeutică standard în cazul acestei afecţiuni în numeroase centre de chirurgie cardiacă4,5.
Prezentare de caz
Prezentăm cazul unui sugar in vârstă de 5 luni, de sex feminin, care este adus spre internare în condiţiile existenţei unei grave distrofii (greutate de 2800g la vârsta de 5 luni) şi a semnelor de insuficienţă cardiacă. La internare starea generală era compromisă, cu polipnee, murmur vezicular înăsprit, fără raluri pulmonare, saturaţia periferică în oxigen: 95%, dedublare fixă de zgomot II, suflu sistolic ejecţional în focarul pulmonarei, abdomen meteorizat şi globulos, ficat cu marginea inferioara palpabilă la 3 cm sub rebordul costal.
Examenele de laborator realizate pentru elucidarea retardului important de creştere au fost negative, negăsindu-se nicio cauza infecţioasă, metabolică sau endocrinologică, iar cariotipul a fost normal.
Ecocardiografia a depistat o malformaţie cardiacă congenitală simplă: defect septal interatrial (DSA) larg, tip ostium secundum, cavităţi drepte mult dilatate (atriu drept, ventricul drept, artera pulmonară), hipertensiune pulmonară (presiune pulmonară medie: 40 mmHg), defect septal interventricular muscular apical mic, insuficienţă mitrală uşoară (Figura 1, 2).
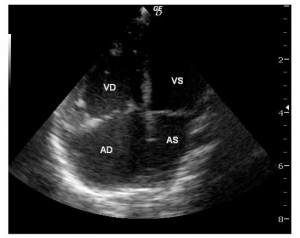
Figura 1. Ecocardiografie transtoracică incidenţă apical 4 camere: dilataţie de cavităţi drepte, defect septal interatrial tip ostium secundum. AD: atriu drept, VD: ventricul drept, AS: atriu stâng, VS: ventricul stâng.
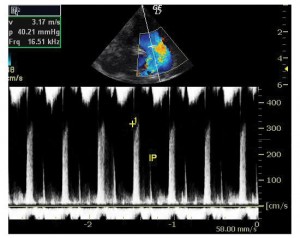
Figura 2. Ecocardiografie transtoracică incidenţă parasternal ax scurt: dilataţie de arteră pulmonară, insuficienţă pulmonară (v max protodiastolică 3,12m/s).
S-a instituit tratament cu inhibitor de enzimă de conversie, furosemid şi spironolactonă, fără a surveni o ameliorare clinică. Atribuind retardul important de creştere doar malformaţiei cardiace, în condiţiile unor investigaţii de laborator negative, sugarul a fost transferat într-un centru de chirurgie cardiacă unde s-a realizat intervenţia chirurgicală corectoare.
Evoluţia imediat postoperatorie a fost fără complicaţii, sugarul revenind în secţia de cardiologie pentru recuperare. Condiţiile generale erau ameliorate, notându-se chiar şi o uşoară creştere ponderală. Controalele ecocardiografice succesive au evidenţiat însă o dilataţie graduală a ventriculului stâng cu afectarea progresivă a funcţiei sistolice şi apariţia ulterioară a unei insuficienţe mitrale severe. Nu a putut fi vizualizată originea arterei coronare stângi din aortă, în plus notându-se flux bidirecţional în artera coronară descendentă anterioară la examenul Doppler color, ridicând suspiciunea de origine anormală a arterei coronare stângi (Figura 3). Presiunea pulmonară se redusese semnificativ (presiunea pulmonară medie a scăzut de la 40 mmHg la 21 mmHg), iar la nivelul septului interatrial nu exista şunt rezidual. Electrocardiograma evidenţia semne de ischemie miocardică, inexistente pe electrocardiogramele de dinainte de intervenţie: segment ST subdenivelat descendent în precordialele stângi şi unde T negative simetrice în precordialele drepte (Figura 4).
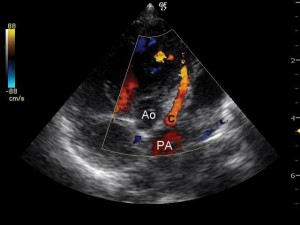
Figura 3. Ecocardiografie transtoracică incidenţă parasternal ax scurt: origine anormală a arterei coronare stângi. Ao: aortă, P: pulmonară, C: artera coronară.
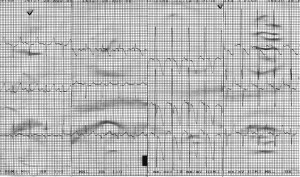
Figura 4. Electrocardiogramă: segment ST subdenivelat descendent în precordialele stângi şi unde T negative simetrice în precordialele drepte.
În aceste condiţii sugarul a fost din nou transferat în serviciul de chirurgie cardiacă. S-a realizat cateterismul cardiac care a confirmat suspiciunea ecocardiografică de origine anormală a arterei coronare stângi din artera pulmonară (Figura 5). S-a reintervenit chirurgical. Intraoperator s-a observat originea arterei coronare stângi la nivelul bifurcaţiei arterei pulmonare, posterior, având un trunchi comun destul de lung. S-a realizat implantarea arterei coronare stângi în aortă. Evoluţia post-reintervenţie a fost bună, cu instalarea unei bune creşteri ponderale ulterior. Ecocardiografia a ilustrat noua origine a arterei coronare stângi din aortă (Figura 6), absenţa şuntului la nivelul septului interatrial şi ventriculul stâng revenit la o contractilitate bună (Figura 7); insuficienţa mitrală era uşoara şi persista defectul septal interventricular muscular apical mic. Electrocardiograma s-a normalizat (Figura 8). La 3 ani de la intervenţie copilul este asimptomatic şi are o dezvoltare psihosomatică corespunzătoare vârstei.
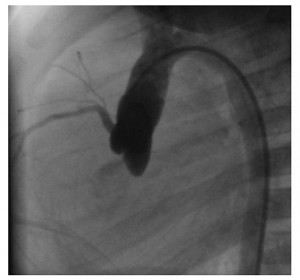
Figura 5. Coronarografie: absenţa originii arterei coronare stângi din aortă.
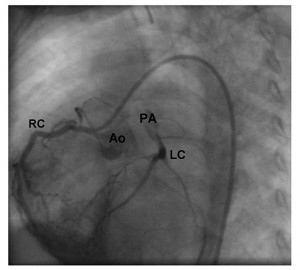
Figura 6. Coronarografie: vizualizarea coronarei stângi prin reinjectare din coronara dreaptă.
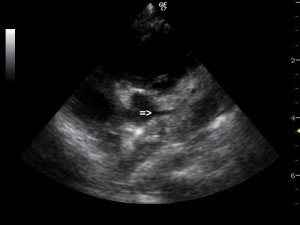
Figura 7. Ecocardiografie transtoracică incidenţă parasternal ax scurt: vizualizarea originii corecte a arterei coronare stângi din aortă.
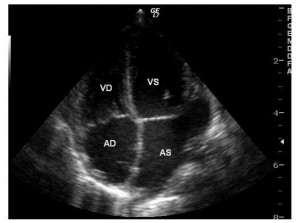
Figura 8. Ecocardiografie transtoracică incidenţă apical 4 camere: dimensiuni normale ale ventriculului stâng, absenţa defectului septal interatrial. AD: atriu drept, VD: ventricul drept, AS: atriu stâng, VS: ventricul stâng.
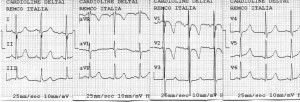
Figura 9. Electrocardiogramă: ritm sinusal 103/minut, fără modificări patologice de repolarizare.
Discuţii şi concluzii
Cazul demonstrează că hiperdebitul pulmonar şi hipertensiunea pulmonară secundare defectului septal interatrial ameliorează sau anulează furtul sanguin din artera coronară stângă către artera pulmonară, “protejând” astfel sugarul de consecinţele ischemice tipice pentru originea anormală a arterei coronare stângi din artera pulmonară, dar întârziind în acelaşi timp diagnosticul corect. Închiderea defectului septal interatrial, cu reducerea consecutivă a presiunii pulmonare, duce la demascarea anomaliei, prin apariţia semnelor şi simptomelor ischemice.
În concluzie, se poate spune că acele condiţii clinice care se asociază cu presiuni pulmonare crescute pot face imposibilă recunoaşterea unei origini anormale a arterei coronare stângi din artera pulmonară, demonstrarea sau nu a originii arterelor coronare trebuind să fie menţionată în mod expres la ecocardiografie.
Bibliografie
1. G. Paul Matherne, MD, D. Scott Lim, MD. Congenital anomalies of the coronary vessels and the aortic root. In Moss and Adams’ Heart disease in infants, children, and adolescents, Seventh edition. Eds: Hugh
d. Allen, MD, ScD( Hon), David J. Driscoll, MD, Robert E. Shaddy, MD,
Timothy F. Feltes, MD, Lippincott Williams & Wilkins, 2008, 703-715.
2. L. Grosse-Wortmann, T. Wenzel, H. H. Hevels-Guerich. Anomalous origin of the left coronary artery from the pulmonary artery in a premature infant with preserved left ventricular function. Pediatr Cardiol 27:269-271, 2006.
3. Robert A Crowles, Walter E Berdon. Bland-White-Garland Syndrome of anomalous left coronary artery arising from the pulmonary artery: a historical review. Pediatr Radiol 2007 37: 890-895.
4. Claire Irving, Christopher Wren. Asymptomatic anomalous origin of the left coronary artery from the pulmonary artery. Pediatr cardiol 2009 30: 385-386.
5. V. T. Tsang, J. Stark. Congenital coronary artery fistula and anomalous origin of the left coronary artery from the pulmonary artery. In Surgery for congenital heart defects, third edition. Eds: Jaroslav F. Stark, Marc R. de Leval, Victor T. Tsang, Wiley, 2006, 612-617.
 This work is licensed under a
This work is licensed under a